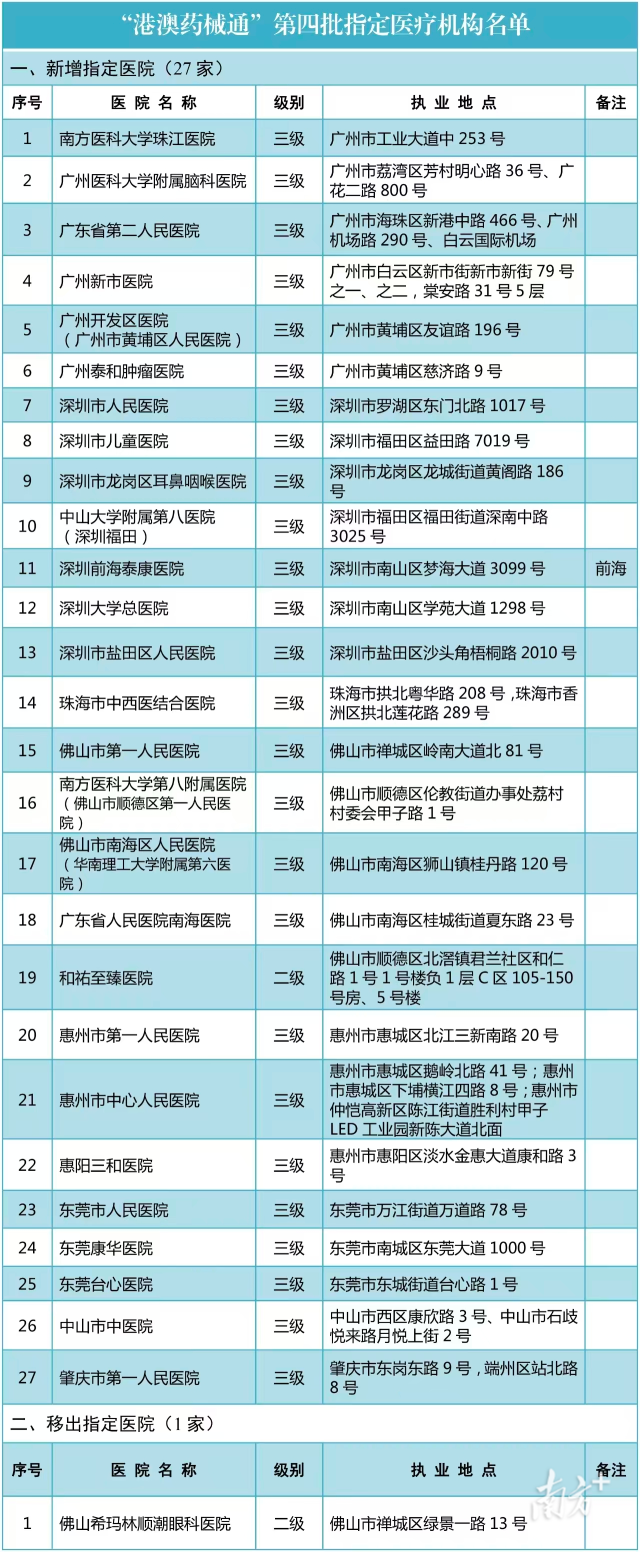
12月8日,粵港澳大灣區醫療融合迎來新進展。廣東省衛生健康委員會與廣東省藥品監督管理局聯合發布通知,正式公布“港澳藥械通”第四批指定醫療機構名單。本次新增27家醫療機構,同時有1家機構被移出名單。
該政策旨在便利大灣區內地居民使用已在港澳上市但未在內地注冊的臨床急需藥品和醫療器械。根據通知,名單的確定依據國家相關工作方案及推進計劃,經由地市評估上報和省級審核后產生。
對于新增的指定醫療機構,通知明確了其主體責任。各機構須嚴格遵守廣東省相關管理條例及工作機制,建立由院領導牽頭負責的制度,深化與港澳的醫療衛生服務合作。同時,醫療機構需優化內部流程,積極申報港澳藥械使用,并建立健全從提報、采購到使用、貯存的全鏈條管理制度,確保藥械來源可溯、去向可追、風險可控。
通知特別強調,各機構必須落實法定代表人承諾制度,保障進口港澳藥械僅用于本機構特定醫療目的,嚴禁非法流入社會,切實保障用藥用械安全,讓群眾享受到更優質、高效、安全的醫療服務。
“港澳藥械通”政策是粵港澳大灣區醫療監管創新發展的重要舉措,通過建立“綠色通道”,滿足了大灣區居民對于前沿藥械的臨床急需。此次指定醫療機構的進一步擴容,標志著該政策覆蓋網絡持續拓寬,大灣區醫療資源加速融合的步伐正在加快。
(記者 唐亞冰 通訊員 粵藥監)
掃一掃,分享到微信朋友圈